脳神経内科における遺伝医療の未来予想図
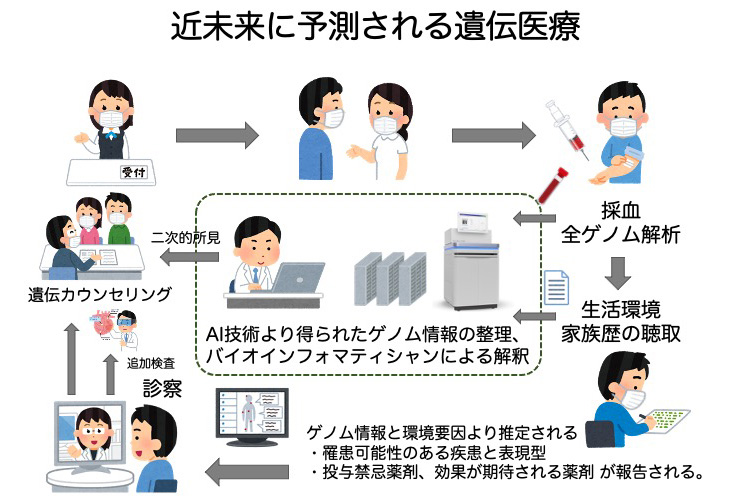
20XX年、そう遠くない未来のY総合病院にて。
患者Aさんは初診受付の後、まず認定遺伝カウンセラーを兼ねるゲノムコーディネーターと面談する。生活環境や家族歴の聴取が行われ、網羅的全ゲノム解析を行うことに同意した後、数ccの採血が行われる。その血液は、次世代シークエンサーが更に進化した近未来シークエンサーによって、イントロンも含めた全ゲノム解析がなされる。30分後には解析が終了し、AIによって初期解析されたデータをもとに、バイオインフォマティシャンが詳細な解釈を加える。採血から1時間後、Aさんが主治医の前に呼ばれた時には、全ゲノム解析によって明らかとなったAさんが罹患する可能性の高い疾患名一覧とその臨床的特徴や、Aさんに投与すると副作用が現れる可能性が高い薬剤リストなどの情報が電子カルテ上にすでに掲載されている(図)。
幾分、私の誇大妄想が入っているかもしれません。さらに妄想を膨らませると、両親の同意下で出生時に全ゲノム解析が行われ、マイナンバーカードにゲノム情報が付加される時代になり、医療機関を受付すると同時にその情報が電子カルテ上に掲載される。。。というような時代になることもあり得るのかもしれません。実際にこのような遺伝医療を行う事が現実に可能になりつつあります。今までの遺伝医療を振り返りつつ、少し今後のことを予想してみましょう。
遺伝医学は、1865年にメンデルによって遺伝法則が発見されたことに始まり、1956年にはヒトの染色体が46本であることが報告され、臨床遺伝診療は始まりました。さらに1980年代後半から、多くの単一遺伝性神経疾患の原因遺伝子が次々と解明され、2003年にはヒトの全ゲノム塩基配列が解明されるに至りました。これにより頻度が高い遺伝性疾患の大部分は原因究明に至りましたが、一般診療の中で遺伝性疾患を診療する機会は少なく、〝遺伝医療=稀少疾患〟というイメージを持つ医療者も多かったものと推測します。しかし2000年代半ばに次世代シークエンサーが登場し、膨大な塩基配列の解読が劇的に速く、かつ低コストで実施できるようになりました。それまでは、臨床症状から疑われる疾患を絞り込み、候補となる原因遺伝子を順に解析していたわけですが、一度の解析で大量の遺伝情報を同時に読み取ることが可能となるという新しい遺伝医療が始まりました。がんゲノム医療や未診断疾患イニシアチブ(IRUD)がその代表例といえます。さらには遺伝性疾患の研究から孤発性疾患の原因究明や治療薬の開発もなされるようになりました (例;大理石骨病研究から見出された骨粗鬆症治療薬デノスマブや遺伝性腎性糖尿病研究からの糖尿病治療薬SGLT2阻害薬)。2015年には内閣官房健康・医療戦略推進本部の下にゲノム医療実現推進協議会が設置され、認知症、難病領域も含めた多様な領域において国家プロジェクトとしてゲノム医療を推進する方針が明示され、2023年6月にはいわゆる“ゲノム医療推進法”も制定されました。次世代シークエンサーは、遺伝医療を遺伝性疾患の診療のみならず、個々の遺伝情報に合わせ個別化医療を提供する診療への転換、すなわち“ゲノムファースト”時代の到来という大きなパラダイムシフトをもたらしました。
現在、新しい病態修飾療法が多数開発され、今まで難治性疾患と言われていた遺伝性神経疾患の一部おいても、早期診断、早期治療が求められる疾患が増えてきました。今後も新しい治療法はどんどん増えることでしょう。疾患の発症には遺伝要因と環境要因が関与することが昔から知られていましたが、今後はそれらに加えて時間的要因を考慮する必要があります。時間的要因を十分に認識して、より早期に遺伝学的検査による診断(確定診断、発症前診断、出生前診断、着床前診断)を含めた遺伝医療が介入することで根治療法に直結する可能性があります。そして、このような医療の進歩は、遺伝領域の究極の目標である個性および多様性を受け入れる社会の実現に向けて大きく貢献することになるでしょう。
冒頭で示したような遺伝医療が実際に行われるためには、遺伝教育や人材育成が極めて重要であることは言うまでもありません。それと同時に医療人を含めた社会の遺伝リテラシーの向上を目指した啓蒙活動を継続していくことも大切です。若い力への期待は大きいです!! (文責 やべっち)